Vollständige Verschreibungsinformationen
Lidocainhydrochlorid-Injektion, USKonservierungsmittelfreie Lidocainhydrochlorid-Injektionslösung
Lidocainhydrochlorid-Injektion USP, 1%
Zur Infiltration und Nervenblockade
Nur Rx
BESCHREIBUNG:
Lidocainhydrochlorid-Injektion, USP ist eine sterile, nicht-pyrogene, wässrige Lösung, die ein Lokalanästhetikum enthält und parenteral durch Injektion verabreicht wird. Siehe INDIKATIONEN für spezifische Anwendungen.
Die Lösung enthält Lidocain HCl, das chemisch als Acetamid, 2-(Diethylamino)-N-(2,6-dimethylphenyl)-, Monohydrochlorid bezeichnet wird und ein Molekulargewicht von 270,8 aufweist. Lidocain HCl (C14H22N2O - HCl) hat die folgende Strukturformel:
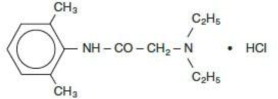
Lidocainhydrochlorid-Injektion, USP Einzeldosislösungen sind frei von Methylparaben.
Lidocainhydrochlorid-Injektion, USP, ist eine sterile, nicht-pyrogene, isotonische Lösung, die Natriumchlorid enthält. Der pH-Wert dieser Lösung wird mit Natriumhydroxid und/oder Salzsäure auf etwa 6,5 (5,0 bis 7,0) eingestellt.
KLINISCHE PHARMAKOLOGIE:
Mechanismus der Wirkung:
Lidocain HCl stabilisiert die Neuronenmembran durch Hemmung der Ionenflüsse, die für die Einleitung und Leitung von Impulsen erforderlich sind, und bewirkt so eine lokale Anästhesiewirkung.
Hämodynamik:
Überhöhte Blutspiegel können zu Veränderungen des Herzzeitvolumens, des gesamten peripheren Widerstands und des mittleren arteriellen Drucks führen. Bei zentraler Nervenblockade können diese Veränderungen auf eine Blockade der autonomen Fasern, eine direkte depressive Wirkung des Lokalanästhetikums auf verschiedene Komponenten des kardiovaskulären Systems und/oder die den beta-adrenergen Rezeptor stimulierende Wirkung von Epinephrin zurückzuführen sein, sofern vorhanden. Der Nettoeffekt ist normalerweise eine leichte Hypotonie, wenn die empfohlenen Dosierungen nicht überschritten werden.
Pharmakokinetik und Metabolismus:
Aus verschiedenen Formulierungen, Konzentrationen und Verwendungen geht hervor, dass Lidocain-HCl nach parenteraler Verabreichung vollständig resorbiert wird, wobei die Resorptionsrate von verschiedenen Faktoren wie dem Verabreichungsort und dem Vorhandensein oder Fehlen eines Vasokonstriktors abhängt. Außer bei intravaskulärer Verabreichung werden die höchsten Blutspiegel nach interkostaler Nervenblockade und die niedrigsten nach subkutaner Verabreichung erreicht.
Die Plasmabindung von Lidocain-HCl hängt von der Wirkstoffkonzentration ab, und die gebundene Fraktion nimmt mit steigender Konzentration ab. Bei Konzentrationen von 1 bis 4 mcg freier Base pro ml sind 60 bis 80 Prozent des Lidocain-HCl proteingebunden. Die Bindung ist auch von der Plasmakonzentration des Alpha-1-Säure-Glykoproteins abhängig.
Lidocain-HCl überwindet die Blut-Hirn-Schranke und die Plazentaschranke, vermutlich durch passive Diffusion.
Lidocain-HCl wird rasch von der Leber metabolisiert, und die Metaboliten sowie das unveränderte Medikament werden über die Nieren ausgeschieden. Die Biotransformation umfasst oxidative N-Dealkylierung, Ringhydroxylierung, Spaltung der Amidbindung und Konjugation. Die N-Dealkylierung, ein Hauptweg der Biotransformation, führt zu den Metaboliten Monoethylglycinexylidid und Glycinexylidid. Die pharmakologischen/toxikologischen Wirkungen dieser Metaboliten ähneln denen von Lidocain-HCl, sind aber weniger stark als diese. Ungefähr 90 % des verabreichten Lidocain-HCl werden in Form verschiedener Metaboliten ausgeschieden, weniger als 10 % werden unverändert ausgeschieden. Der Hauptmetabolit im Urin ist ein Konjugat von 4-Hydroxy-2,6-dimethylanilin.
Die Eliminationshalbwertszeit von Lidocain-HCl nach einer intravenösen Bolusinjektion beträgt typischerweise 1,5 bis 2 Stunden. Aufgrund der schnellen Metabolisierung von Lidocain-HCl kann jeder Zustand, der die Leberfunktion beeinträchtigt, die Lidocain-HCl-Kinetik verändern. Die Halbwertszeit kann sich bei Patienten mit Leberfunktionsstörungen um das Zweifache oder mehr verlängern. Nierenfunktionsstörungen haben keinen Einfluss auf die Kinetik von Lidocain-HCl, können aber die Akkumulation von Metaboliten erhöhen.
Faktoren wie Azidose und die Einnahme von ZNS-Stimulanzien und Depressiva beeinflussen die ZNS-Spiegel von Lidocain-HCl, die erforderlich sind, um offene systemische Wirkungen hervorzurufen. Objektive unerwünschte Wirkungen werden mit zunehmenden venösen Plasmaspiegeln von mehr als 6 mcg freier Base pro mL immer deutlicher. Beim Rhesusaffen haben sich arterielle Blutspiegel von 18 bis 21 mcg/ml als Schwellenwert für krampfartige Aktivität erwiesen.
INDIKATIONEN UND VERWENDUNG:
Lidocainhydrochlorid-Injektion, USP, ist für die Erzeugung von Lokal- oder Regionalanästhesie durch Infiltrationstechniken wie perkutane Injektion und intravenöse Regionalanästhesie durch periphere Nervenblocktechniken wie Brachialplexus- und Interkostalblock und durch zentrale Nervenblocktechniken wie lumbale und kaudale Epiduralblockaden indiziert, wenn die anerkannten Verfahren für diese Techniken, wie sie in Standardlehrbüchern beschrieben sind, eingehalten werden.
KONTRAINDIKATIONEN:
Lidocain HCl ist kontraindiziert bei Patienten mit einer bekannten Überempfindlichkeit gegen Lokalanästhetika des Amidtyps.
WARNUNGEN:
LIDOCAIN-HYDROCHLORID-INJEKTION, USP ZUR INFILTRATION UND NERVENBLOCKADE SOLLTE NUR VON KLINIKERN VERWENDET WERDEN, DIE IN DER DIAGNOSE UND BEHANDLUNG VON DOSISBEDINGTEN TOXIZITÄTEN UND ANDEREN AKUTEN NOTFÄLLEN, DIE SICH AUS DER ZU VERWENDENDEN BLOCKADE ERGEBEN KÖNNEN, VERSIERT SIND, UND AUCH NUR DANN, WENN DIE SOFORTIGE VERFÜGBARKEIT VON SAUERSTOFF SICHERGESTELLT IST, ANDERE RESUSZITATIVE ARZNEIMITTEL, KARDIOPULMONÄRE AUSRÜSTUNG UND PERSONAL, das für die ordnungsgemäße Behandlung von toxischen Reaktionen und damit verbundenen Notfällen erforderlich ist (siehe auch ANWENDUNGEN und VORSICHTSMASSNAHMEN). EINE VERZÖGERTE BEHANDLUNG DER DOSISBEDINGTEN TOXIZITÄT, UNTERBELÜFTUNG JEGLICHER URSACHE UND/ODER VERÄNDERTE EMPFINDLICHKEIT KÖNNEN ZUR ENTWICKLUNG EINER ACIDOSE, EINES HERZSTILLSTANDS UND MÖGLICHERWEISE ZUM TOD FÜHREN.
Hämoglobinämie
Fälle von Methämoglobinämie sind im Zusammenhang mit der Anwendung von Lokalanästhetika berichtet worden. Obwohl bei allen Patienten ein Risiko für Methämoglobinämie besteht, sind Patienten mit Glukose-6-Phosphat-Dehydrogenase-Mangel, angeborener oder idiopathischer Methämoglobinämie, Herz- oder Lungenproblemen, Säuglingen unter 6 Monaten und gleichzeitiger Exposition gegenüber Oxidationsmitteln oder deren Metaboliten anfälliger für die Entwicklung klinischer Manifestationen des Zustands. Wenn Lokalanästhetika bei diesen Patienten angewendet werden müssen, wird eine genaue Überwachung auf Symptome und Anzeichen einer Methämoglobinämie empfohlen.
Die Anzeichen einer Methämoglobinämie können sofort auftreten oder einige Stunden nach der Exposition verzögert werden und sind durch eine zyanotische Hautverfärbung und/oder eine abnorme Färbung des Blutes gekennzeichnet. Die Methämoglobinwerte können weiter ansteigen; daher ist eine sofortige Behandlung erforderlich, um schwerwiegendere unerwünschte Wirkungen auf das zentrale Nervensystem und das Herz-Kreislauf-System, einschließlich Krampfanfällen, Koma, Herzrhythmusstörungen und Tod, abzuwenden. Lidocain HCl Injektion, USP und andere Oxidationsmittel absetzen. Je nach Schwere der Anzeichen und Symptome können die Patienten auf eine unterstützende Behandlung ansprechen, z. B. Sauerstofftherapie und Flüssigkeitszufuhr. Ein schwereres klinisches Bild kann eine Behandlung mit Methylenblau, Austauschtransfusion oder hyperbarem Sauerstoff erfordern.
Intraartikuläre Infusionen von Lokalanästhetika nach arthroskopischen und anderen chirurgischen Eingriffen sind eine nicht zugelassene Anwendung, und es gibt Berichte über Chondrolyse bei Patienten, die solche Infusionen erhalten haben, nach dem Inverkehrbringen. Die Mehrzahl der gemeldeten Fälle von Chondrolyse betraf das Schultergelenk; Fälle von glenohumeraler Chondrolyse wurden bei pädiatrischen und erwachsenen Patienten nach intraartikulären Infusionen von Lokalanästhetika mit und ohne Epinephrin über einen Zeitraum von 48 bis 72 Stunden beschrieben. Es liegen keine ausreichenden Informationen vor, um festzustellen, ob kürzere Infusionszeiten nicht mit diesen Befunden einhergehen. Der Zeitpunkt des Auftretens von Symptomen wie Gelenkschmerzen, Steifheit und Bewegungseinschränkung kann unterschiedlich sein, kann aber bereits im zweiten Monat nach der Operation beginnen. Monat nach der Operation beginnen. Derzeit gibt es keine wirksame Behandlung für Chondrolyse; bei Patienten mit Chondrolyse waren zusätzliche diagnostische und therapeutische Verfahren erforderlich, und bei einigen war eine Arthroplastik oder ein Schulterersatz notwendig.
Um eine intravaskuläre Injektion zu vermeiden, sollte vor der Injektion der Lokalanästhesielösung eine Aspiration durchgeführt werden. Die Nadel muss so lange neu positioniert werden, bis durch Aspiration kein Blut mehr zurückfließt. Beachten Sie jedoch, dass die Abwesenheit von Blut in der Spritze keine Garantie dafür ist, dass eine intravaskuläre Injektion vermieden wurde.
Lokalanästhesielösungen, die antimikrobielle Konservierungsmittel (z. B. Methylparaben) enthalten, sollten nicht für die Epidural- oder Spinalanästhesie verwendet werden, da die Sicherheit dieser Mittel im Hinblick auf eine absichtliche oder versehentliche intrathekale Injektion nicht nachgewiesen wurde.
Lidocain HCl mit Epinephrin-Lösungen enthalten Natriummetabisulfit, ein Sulfit, das bei bestimmten empfänglichen Personen allergische Reaktionen einschließlich anaphylaktischer Symptome und lebensbedrohliche oder weniger schwere asthmatische Episoden hervorrufen kann. Die Gesamtprävalenz der Sulfit-Empfindlichkeit in der Allgemeinbevölkerung ist unbekannt und wahrscheinlich gering. Eine Sulfit-Empfindlichkeit wird häufiger bei Asthmatikern als bei Nicht-Asthmatikern beobachtet.
Nach Verabreichung von Lidocainhydrochlorid können anaphylaktische Reaktionen auftreten (siehe UNERWÜNSCHTE REAKTIONEN).
Im Falle einer schweren Reaktion ist die Einnahme des Arzneimittels abzubrechen.
VORSICHTSMASSNAHMEN:
Allgemein
Die Sicherheit und Wirksamkeit von Lidocain-HCl hängen von der richtigen Dosierung, der korrekten Technik, angemessenen Vorsichtsmaßnahmen und der Bereitschaft für Notfälle ab. Standardlehrbücher sollten für spezifische Techniken und Vorsichtsmaßnahmen für verschiedene Regionalanästhesieverfahren konsultiert werden.
Wiederbelebungsgeräte, Sauerstoff und andere Wiederbelebungsmittel sollten für den sofortigen Einsatz zur Verfügung stehen. (Siehe WARNHINWEISE und UNERWÜNSCHTE REAKTIONEN). Die niedrigste Dosierung, die zu einer wirksamen Anästhesie führt, sollte verwendet werden, um hohe Plasmaspiegel und schwerwiegende unerwünschte Wirkungen zu vermeiden. Bei der Anwendung von Dauerkathetertechniken sollten vor und während jeder zusätzlichen Injektion Spritzenaspirationen durchgeführt werden. Bei der Verabreichung einer Epiduralanästhesie wird empfohlen, zunächst eine Testdosis zu verabreichen und den Patienten auf Toxizität für das zentrale Nervensystem und kardiovaskuläre Toxizität sowie auf Anzeichen einer unbeabsichtigten intrathekalen Verabreichung zu überwachen, bevor die Behandlung fortgesetzt wird. Wenn die klinischen Bedingungen es zulassen, sollte erwogen werden, für die Testdosis epinephrinhaltige Lokalanästhesielösungen zu verwenden, da mit Epinephrin kompatible Kreislaufveränderungen auch als Warnzeichen für eine unbeabsichtigte intravasale Injektion dienen können. Eine intravaskuläre Injektion ist auch dann möglich, wenn die Aspiration von Blut negativ ist. Wiederholte Gaben von Lidocain-HCl können aufgrund der langsamen Akkumulation des Arzneimittels oder seiner Metaboliten bei jeder wiederholten Gabe zu einem erheblichen Anstieg der Blutspiegel führen. Die Toleranz gegenüber erhöhten Blutspiegeln variiert mit dem Zustand des Patienten. Geschwächte, ältere Patienten, akut kranke Patienten und Kinder sollten eine ihrem Alter und ihrer körperlichen Verfassung entsprechende, reduzierte Dosis erhalten. Lidocain HCl sollte auch bei Patienten mit schwerem Schock oder Herzblock mit Vorsicht angewendet werden.
Die lumbale und kaudale Epiduralanästhesie sollte bei Personen mit folgenden Erkrankungen mit äußerster Vorsicht angewendet werden: bestehende neurologische Erkrankungen, Wirbelsäulendeformitäten, Septikämie und schwerer Bluthochdruck.
Lokalanästhesielösungen, die einen Vasokonstriktor enthalten, sollten in Körperregionen, die von Endarterien versorgt werden oder deren Blutversorgung anderweitig beeinträchtigt ist, mit Vorsicht und in sorgfältig abgegrenzten Mengen verwendet werden. Patienten mit peripheren Gefäßerkrankungen und Patienten mit hypertensiven Gefäßerkrankungen können eine übermäßige Vasokonstriktorreaktion aufweisen. Ischämische Verletzungen oder Nekrosen können die Folge sein. Präparate, die einen Vasokonstriktor enthalten, sollten bei Patienten während oder nach der Verabreichung starker Allgemeinanästhetika mit Vorsicht angewendet werden, da unter diesen Bedingungen Herzrhythmusstörungen auftreten können.
Nach jeder Injektion eines Lokalanästhetikums sollte eine sorgfältige und ständige Überwachung der kardiovaskulären und respiratorischen Vitalzeichen (Angemessenheit der Beatmung) sowie des Bewusstseinszustandes des Patienten durchgeführt werden. Dabei ist zu beachten, dass Unruhe, Angst, Tinnitus, Schwindel, verschwommenes Sehen, Zittern, Depression oder Schläfrigkeit frühe Warnzeichen für eine Toxizität des zentralen Nervensystems sein können.
Da Lokalanästhetika vom Amid-Typ durch die Leber metabolisiert werden, sollte Lidocainhydrochlorid-Injektion, USP bei Patienten mit Lebererkrankungen mit Vorsicht angewendet werden. Patienten mit schwerer Lebererkrankung sind aufgrund ihrer Unfähigkeit, Lokalanästhetika normal zu metabolisieren, einem größeren Risiko ausgesetzt, toxische Plasmakonzentrationen zu entwickeln. Lidocainhydrochlorid-Injektion, USP sollte auch mit Vorsicht bei Patienten mit eingeschränkter kardiovaskulärer Funktion verwendet werden, da sie weniger in der Lage sein können, funktionelle Veränderungen zu kompensieren, die mit der Verlängerung der A-V-Leitung durch diese Medikamente verbunden sind.
Viele Medikamente, die bei der Durchführung einer Anästhesie verwendet werden, gelten als potenzielle Auslöser einer familiären malignen Hyperthermie. Da nicht bekannt ist, ob Lokalanästhetika vom Amid-Typ diese Reaktion auslösen können, und da die Notwendigkeit einer zusätzlichen Vollnarkose nicht im Voraus vorhergesagt werden kann, wird vorgeschlagen, ein Standardprotokoll für das Management der malignen Hyperthermie zu erstellen. Frühe unerklärliche Anzeichen wie Tachykardie, Tachypnoe, labiler Blutdruck und metabolische Azidose können einem Temperaturanstieg vorausgehen. Der Erfolg hängt von einer frühzeitigen Diagnose, dem unverzüglichen Absetzen des/der verdächtigen Auslöser(s) und der Einleitung einer Behandlung ab, die eine Sauerstofftherapie, indizierte unterstützende Maßnahmen und Dantrolen einschließt (lesen Sie vor der Anwendung die Packungsbeilage von Dantrolen-Natrium intravenös).
Eine korrekte Tourniquet-Technik, wie sie in Veröffentlichungen und Standardlehrbüchern beschrieben wird, ist für die Durchführung einer intravenösen Regionalanästhesie unerlässlich. Lösungen, die Epinephrin oder andere Vasokonstriktoren enthalten, sollten für diese Technik nicht verwendet werden.
Lidocain HCl sollte bei Personen mit bekannten Arzneimittelüberempfindlichkeiten mit Vorsicht angewendet werden. Bei Patienten, die auf para-Aminobenzoesäure-Derivate (Procain, Tetracain, Benzocain usw.) allergisch reagieren, wurde keine Kreuzsensitivität gegenüber Lidocain HCl festgestellt.
Anwendung im Kopf- und Halsbereich
Kleine Dosen von Lokalanästhetika, die in den Kopf- und Halsbereich injiziert werden, einschließlich retrobulbärer, zahnärztlicher und stellater Ganglion-Blockaden, können zu Nebenwirkungen führen, die mit der systemischen Toxizität vergleichbar sind, die bei unbeabsichtigten intravaskulären Injektionen größerer Dosen beobachtet wird. Verwirrtheit, Krämpfe, Atemdepression und/oder Atemstillstand sowie kardiovaskuläre Stimulation oder Depression sind berichtet worden. Diese Reaktionen können auf die intraarterielle Injektion des Lokalanästhetikums mit retrogradem Fluss in den zerebralen Kreislauf zurückzuführen sein. Bei Patienten, die diese Blöcke erhalten, sollten Kreislauf und Atmung überwacht und ständig beobachtet werden. Wiederbelebungsgeräte und Personal zur Behandlung von Nebenwirkungen sollten sofort verfügbar sein. Die Dosierungsempfehlungen sollten nicht überschritten werden (siehe ANWENDUNG UND VERABREICHUNG).
Informationen für Patienten
Gegebenenfalls sollten die Patienten im Voraus darüber informiert werden, dass sie nach der ordnungsgemäßen Verabreichung einer Epiduralanästhesie eine vorübergehende Beeinträchtigung des Gefühls und der motorischen Aktivität, gewöhnlich in der unteren Körperhälfte, erfahren können.
Klinisch bedeutsame Wechselwirkungen mit Medikamenten
Die Verabreichung von epinephrin- oder norepinephrinhaltigen Lokalanästhesielösungen an Patienten, die Monoaminoxidase-Hemmer oder trizyklische Antidepressiva erhalten, kann zu schwerem, lang anhaltendem Bluthochdruck führen.
Phenothiazine und Butyrophenone können die pressorische Wirkung von Epinephrin verringern oder umkehren.
Die gleichzeitige Anwendung dieser Mittel sollte generell vermieden werden. In Situationen, in denen eine gleichzeitige Therapie notwendig ist, ist eine sorgfältige Überwachung des Patienten unerlässlich.
Die gleichzeitige Verabreichung von vasopressorischen Arzneimitteln (zur Behandlung von Hypotonie im Zusammenhang mit Geburtsblockaden) und Mutterkorn-haltigen Oxytocika kann zu schwerem, anhaltendem Bluthochdruck oder zerebrovaskulären Unfällen führen.
Wechselwirkungen zwischen Medikamenten und Labortests
Die intramuskuläre Injektion von Lidocain-HCl kann zu einem Anstieg des Kreatinphosphokinase-Spiegels führen. Daher kann die Verwendung dieser Enzymbestimmung ohne Isoenzymtrennung als diagnostischer Test für das Vorliegen eines akuten Myokardinfarkts durch die intramuskuläre Injektion von Lidocain-HCl beeinträchtigt werden.
Bei Patienten, denen Lokalanästhetika verabreicht werden, besteht ein erhöhtes Risiko der Entwicklung einer Methämoglobinämie, wenn sie gleichzeitig den folgenden Arzneimitteln ausgesetzt sind, zu denen auch andere Lokalanästhetika gehören können:
Beispiele für Medikamente, die mit Methämoglobinämie in Verbindung gebracht werden:
| Nitrate/Nitriten | Stickstoffmonoxid, Nitroglyzerin, Nitroprussid, Distickstoffmonoxid |
| Lokale Anästhetika | Artican, Benzocain, Bupivacain, Lidocain, Mepivacain, Prilocain, Procain, Ropivacain, Tetracain |
| Antineoplastische Mittel | Cyclophosphamid, Flutamid, Hydroxyharnstoff, Ifosfamid, Rasburicase |
| Antibiotika | Dapson, Nitrofurantoin, Para-Aminosalicylsäure, Sulfonamide |
| Antimalariamittel | Choloroquin, Primaquin |
| Antikonvulsiva | Phenobarbital, Phenytoin, Natriumvalproat |
| Andere Drogen | Acetaminophen, Metoclopramid, Chinin, Sulfasalazin |
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Tierversuche mit Lidocain-HCl zur Bewertung des karzinogenen und mutagenen Potenzials oder der Auswirkungen auf die Fruchtbarkeit wurden nicht durchgeführt.
Schwangerschaft
Teratogene Wirkungen: Schwangerschaftskategorie B.
Reproduktionsstudien wurden an Ratten mit Dosen bis zum 6,6-fachen der menschlichen Dosis durchgeführt und ergaben keine Hinweise auf eine Schädigung des Fötus durch Lidocain-HCl. Es gibt jedoch keine angemessenen und gut kontrollierten Studien an schwangeren Frauen. Reproduktionsstudien an Tieren sind nicht immer aussagekräftig für die Reaktion beim Menschen. Diese Tatsache sollte generell berücksichtigt werden, bevor Lidocain-HCl an Frauen im gebärfähigen Alter verabreicht wird, insbesondere in der Frühschwangerschaft, wenn die maximale Organogenese stattfindet.
Labor und Entbindung
Lokalanästhetika passieren rasch die Plazenta und können bei Anwendung zur Epidural-, Parazervikal-, Pudendal- oder Kaudalblockanästhesie unterschiedliche Grade mütterlicher, fetaler und neonataler Toxizität verursachen. (siehe KLINISCHE PHARMAKOLOGIE, Pharmakokinetik und Metabolismus). Das Toxizitätspotenzial hängt von dem durchgeführten Verfahren, der Art und Menge des verwendeten Arzneimittels und der Technik der Arzneimittelverabreichung ab. Unerwünschte Wirkungen bei der Gebärenden, dem Fötus und dem Neugeborenen betreffen Veränderungen des zentralen Nervensystems, des peripheren Gefäßtonus und der Herzfunktion.
Mütterliche Hypotonie ist eine Folge der Regionalanästhesie. Lokalanästhetika bewirken eine Vasodilatation durch Blockierung der Sympathikusnerven. Das Hochlegen der Beine und die Lagerung der Patientin auf der linken Seite helfen, einen Blutdruckabfall zu verhindern.
Auch die Herzfrequenz des Fötus sollte kontinuierlich überwacht werden, wobei eine elektronische Überwachung des Fötus sehr zu empfehlen ist.
Epidural-, Spinal-, Parazervikal- oder Pudendalanästhesie können die Geburtskräfte durch Veränderungen der Uteruskontraktilität oder der mütterlichen Ausstoßkräfte verändern. In einer Studie wurde eine parazervikale Blockanästhesie mit einer Verkürzung der durchschnittlichen Dauer der ersten Phase der Wehen und einer Erleichterung der zervikalen Dilatation in Verbindung gebracht. Es wurde jedoch auch berichtet, dass Spinal- und Epiduralanästhesie die zweite Phase der Wehen verlängern können, indem sie den reflexartigen Drang der Gebärenden nach unten ausschalten oder die motorischen Funktionen beeinträchtigen. Die Anwendung von Geburtshilfeanästhesie kann den Bedarf an Zangenhilfe erhöhen.
Die Anwendung einiger Lokalanästhetika während der Wehen und der Geburt kann in den ersten ein bis zwei Lebenstagen zu einer verminderten Muskelkraft und einem verminderten Muskeltonus führen. Die langfristige Bedeutung dieser Beobachtungen ist unbekannt. Eine fetale Bradykardie kann bei 20 bis 30 Prozent der Patientinnen auftreten, die eine parazervikale Nervenblockade mit Lokalanästhetika vom Amid-Typ erhalten, und kann mit einer fetalen Azidose verbunden sein. Die fetale Herzfrequenz sollte während der parazervikalen Anästhesie stets überwacht werden. Der Arzt sollte die möglichen Vorteile gegen die Risiken abwägen, wenn er einen parazervikalen Block bei Frühgeburtlichkeit, Schwangerschaftstoxikose und fetaler Notlage in Betracht zieht. Die sorgfältige Einhaltung der empfohlenen Dosierung ist bei der parazervikalen Anästhesie in der Geburtshilfe von größter Bedeutung. Wird mit den empfohlenen Dosen keine ausreichende Analgesie erreicht, sollte der Verdacht auf eine intravaskuläre oder fetale intrakranielle Injektion geäußert werden. Es wurden Fälle berichtet, die mit einer unbeabsichtigten fetalen intrakraniellen Injektion von Lokalanästhesielösung nach einer beabsichtigten parazervikalen oder pudendalen Blockade oder beidem vereinbar sind. Die betroffenen Säuglinge weisen bei der Geburt eine unerklärliche neonatale Depression auf, die mit hohen Serumspiegeln des Lokalanästhetikums korreliert, und zeigen häufig innerhalb von sechs Stunden Krampfanfälle. Die sofortige Anwendung von Unterstützungsmaßnahmen in Kombination mit der forcierten Ausscheidung des Lokalanästhetikums über den Urin hat sich als erfolgreiches Mittel zur Behandlung dieser Komplikation erwiesen.
Fallberichte über mütterliche Krämpfe und kardiovaskuläre Zusammenbrüche nach der Anwendung einiger Lokalanästhetika für die parazervikale Blockade in der Frühschwangerschaft (als Anästhesie für den Schwangerschaftsabbruch) deuten darauf hin, dass die systemische Absorption unter diesen Umständen schnell erfolgen kann. Die empfohlene Höchstdosis der einzelnen Arzneimittel sollte nicht überschritten werden. Die Injektion sollte langsam und mit häufiger Aspiration erfolgen. Zwischen den einzelnen Injektionen sollte ein Abstand von 5 Minuten eingehalten werden.
Stillende Mütter
Es ist nicht bekannt, ob dieses Arzneimittel in die Muttermilch ausgeschieden wird. Da viele Arzneimittel in die Muttermilch ausgeschieden werden, ist bei der Verabreichung von Lidocain HCl an eine stillende Frau Vorsicht geboten.
Pädiatrische Verwendung
Die Dosierung bei Kindern sollte je nach Alter, Körpergewicht und körperlicher Verfassung reduziert werden (siehe ANWENDUNG UND VERABREICHUNG).
UNERWÜNSCHTE REAKTIONEN
Systemisch
Unerwünschte Wirkungen nach der Verabreichung von Lidocain HCl ähneln denen, die bei anderen Amid-Lokalanästhetika beobachtet werden. Diese unerwünschten Wirkungen sind im Allgemeinen dosisabhängig und können aus hohen Plasmaspiegeln resultieren, die durch eine übermäßige Dosierung, eine schnelle Resorption oder eine versehentliche intravaskuläre Injektion verursacht werden, oder sie können aus einer Überempfindlichkeit, einer Idiosynkrasie oder einer verminderten Toleranz seitens des Patienten resultieren. Schwerwiegende unerwünschte Wirkungen sind im Allgemeinen systemischer Natur. Die folgenden Arten sind die am häufigsten gemeldeten:
Zentrales Nervensystem
ZNS-Manifestationen sind erregend und/oder depressiv und können gekennzeichnet sein durch Benommenheit, Nervosität, Besorgnis, Euphorie, Verwirrung, Schwindel, Schläfrigkeit, Tinnitus, verschwommenes oder doppeltes Sehen, Erbrechen, Hitze-, Kälte- oder Taubheitsgefühle, Zuckungen, Zittern, Krämpfe, Bewusstlosigkeit, Atemdepression und Atemstillstand. Die Erregungserscheinungen können sehr kurz sein oder überhaupt nicht auftreten; in diesem Fall kann die erste Erscheinung der Toxizität Schläfrigkeit sein, die in Bewusstlosigkeit und Atemstillstand übergeht.
Schläfrigkeit nach der Verabreichung von Lidocain-HCl ist in der Regel ein frühes Anzeichen für einen hohen Blutspiegel des Arzneimittels und kann als Folge einer schnellen Resorption auftreten.
Kardiovaskuläres System
Die kardiovaskulären Manifestationen sind in der Regel depressiv und zeichnen sich durch Bradykardie, Hypotonie und kardiovaskulären Kollaps aus, der zum Herzstillstand führen kann.
Allergisch
Allergische Reaktionen sind gekennzeichnet durch Hautläsionen, Urtikaria, Ödeme oder anaphylaktoide Reaktionen. Allergische Reaktionen können als Folge einer Überempfindlichkeit entweder gegenüber Lokalanästhetika oder gegenüber dem Methylparaben auftreten, das als Konservierungsmittel in den Mehrfachdosis-Fläschchen verwendet wird. Allergische Reaktionen, einschließlich anaphylaktischer Reaktionen, können als Folge einer Überempfindlichkeit gegenüber Lidocain auftreten, sind jedoch selten. Wenn allergische Reaktionen auftreten, sollten sie mit konventionellen Mitteln behandelt werden. Der Nachweis der Empfindlichkeit durch Hauttests ist von zweifelhaftem Wert.
Es liegen keine Berichte über eine Kreuzsensitivität zwischen Lidocainhydrochlorid und Procainamid oder zwischen Lidocainhydrochlorid und Chinidin vor.
Neurologisch
Das Auftreten von Nebenwirkungen im Zusammenhang mit der Anwendung von Lokalanästhetika kann mit der Gesamtdosis des verabreichten Lokalanästhetikums zusammenhängen und hängt auch von dem verwendeten Medikament, dem Verabreichungsweg und dem Gesundheitszustand des Patienten ab. In einer prospektiven Untersuchung von 10.440 Patienten, die Lidocain HCl für eine Spinalanästhesie erhielten, wurde die Häufigkeit von unerwünschten Wirkungen mit jeweils etwa 3 Prozent für lagebedingte Kopfschmerzen, Hypotonie und Rückenschmerzen, 2 Prozent für Schüttelfrost und jeweils weniger als 1 Prozent für periphere Nervensymptome, Übelkeit, Atemnot und Doppelbilder angegeben. Viele dieser Beobachtungen können mit den Techniken der Lokalanästhesie zusammenhängen, mit oder ohne Beitrag des Lokalanästhetikums.
In der Praxis der kaudalen oder lumbalen Epiduralblockade kann es gelegentlich zu einem unbeabsichtigten Eindringen des Katheters in den Subarachnoidalraum kommen. Die anschließenden unerwünschten Wirkungen können teilweise von der Menge des subdural verabreichten Arzneimittels abhängen. Dazu gehören eine mehr oder weniger starke Blockade der Wirbelsäule (einschließlich einer totalen Blockade der Wirbelsäule), eine Hypotonie infolge der Blockade der Wirbelsäule, ein Verlust der Kontrolle über Blase und Darm sowie ein Verlust der perinealen Empfindung und der sexuellen Funktion. Anhaltende motorische, sensorische und/oder autonome (Schließmuskelkontrolle) Defizite einiger unterer Wirbelsäulensegmente mit langsamer Erholung (mehrere Monate) oder unvollständiger Erholung wurden in seltenen Fällen berichtet, wenn eine kaudale oder lumbale Epiduralblockade versucht wurde. Nach der Anwendung dieser Anästhesieverfahren wurden auch Rücken- und Kopfschmerzen festgestellt.
Es wurde von Fällen berichtet, in denen nach einer retrobulbären Verabreichung dauerhafte Verletzungen der extraokularen Muskeln auftraten, die eine chirurgische Reparatur erforderten.
Hämatologisches
Methämoglobinämie.
ÜBERDOSIERUNG
Akute Notfälle durch Lokalanästhetika stehen im Allgemeinen im Zusammenhang mit hohen Plasmaspiegeln, die bei der therapeutischen Anwendung von Lokalanästhetika auftreten, oder mit einer unbeabsichtigten subarachnoidalen Injektion von Lokalanästhesielösung (siehe UNERWÜNSCHTE REAKTIONEN, WARNUNGEN und VORSICHTSMASSNAHMEN).
Management von Notfällen bei lokaler Anästhesie
An erster Stelle steht die Vorbeugung, die am besten durch eine sorgfältige und ständige Überwachung der kardiovaskulären und respiratorischen Vitalzeichen und des Bewusstseinszustandes des Patienten nach jeder Lokalanästhesie-Injektion erreicht wird. Bei den ersten Anzeichen einer Veränderung sollte Sauerstoff verabreicht werden.
Der erste Schritt bei der Behandlung von Krämpfen sowie von Unterbeatmung oder Apnoe aufgrund einer unbeabsichtigten subarachnoidalen Injektion von Medikamentenlösung besteht in der sofortigen Aufrechterhaltung eines offenen Atemwegs und einer assistierten oder kontrollierten Beatmung mit Sauerstoff und einem System, das einen sofortigen positiven Atemwegsdruck per Maske ermöglicht. Unmittelbar nach Einleitung dieser Beatmungsmaßnahmen sollte die Angemessenheit des Kreislaufs überprüft werden, wobei zu berücksichtigen ist, dass intravenös verabreichte Medikamente zur Behandlung von Krämpfen manchmal den Kreislauf unterdrücken. Sollten die Krämpfe trotz adäquater Atemunterstützung anhalten und der Zustand des Kreislaufs dies zulassen, können kleine Mengen eines ultrakurz wirksamen Barbiturats (wie Thiopental oder Thiamylal) oder eines Benzodiazepins (wie Diazepam) intravenös verabreicht werden. Der Kliniker sollte vor der Anwendung von Lokalanästhetika mit diesen krampflösenden Medikamenten vertraut sein. Die unterstützende Behandlung einer Kreislaufdepression kann die Verabreichung von intravenöser Flüssigkeit und gegebenenfalls eines Vasopressors je nach klinischer Situation (z. B. Ephedrin) erfordern.
Wenn sie nicht sofort behandelt werden, können sowohl Krämpfe als auch eine kardiovaskuläre Depression zu Hypoxie, Azidose, Bradykardie, Arrhythmien und Herzstillstand führen. Unterbelüftung oder Apnoe aufgrund einer unbeabsichtigten subarachnoidalen Injektion von Lokalanästhesielösung können die gleichen Symptome hervorrufen und ebenfalls zu einem Herzstillstand führen, wenn keine Beatmungsunterstützung eingeleitet wird. Sollte es zu einem Herzstillstand kommen, sollten die üblichen kardiopulmonalen Wiederbelebungsmaßnahmen eingeleitet werden.
Eine endotracheale Intubation unter Verwendung von Medikamenten und Techniken, die dem Arzt vertraut sind, kann nach der anfänglichen Verabreichung von Sauerstoff über eine Maske angezeigt sein, wenn Schwierigkeiten bei der Aufrechterhaltung eines offenen Atemwegs auftreten oder wenn eine längere Beatmungsunterstützung (assistiert oder kontrolliert) angezeigt ist.
Die Dialyse ist von vernachlässigbarem Wert bei der Behandlung einer akuten Überdosierung mit Lidocain-HCl. Die orale LD50 von Lidocain-HCl beträgt bei nicht nüchternen weiblichen Ratten 459 (346 bis 773) mg/kg (als Salz) und 214 (159 bis 324) mg/kg (als Salz) bei nüchternen weiblichen Ratten.
DOSIERUNG UND VERABREICHUNG
In Tabelle 1 (Empfohlene Dosierungen) sind die empfohlenen Volumina und Konzentrationen von Lidocainhydrochlorid-Injektion, USP, für verschiedene Arten von Anästhesieverfahren zusammengefasst. Die in dieser Tabelle empfohlenen Dosierungen gelten für normale gesunde Erwachsene und beziehen sich auf die Verwendung von epinephrinhaltigen Lösungen. Wenn größere Volumina erforderlich sind, sollten nur epinephrinhaltige Lösungen verwendet werden, außer in Fällen, in denen vasopressorische Medikamente kontraindiziert sind.
Bei Patienten, die nach arthroskopischen und anderen chirurgischen Eingriffen intraartikuläre Infusionen von Lokalanästhetika erhalten haben, wurde über unerwünschte Ereignisse wie Chondrolyse berichtet. Lidocainhydrochlorid-Injektion, USP ist für diese Anwendung nicht zugelassen (siehe WARNHINWEISE und ANWENDUNG UND VERABREITUNG).
Diese empfohlenen Dosen dienen lediglich als Richtwert für die Menge des Anästhetikums, die für die meisten Routineeingriffe erforderlich ist. Die tatsächlich zu verwendenden Volumina und Konzentrationen hängen von einer Reihe von Faktoren ab, wie z. B. Art und Umfang des chirurgischen Eingriffs, Tiefe der Anästhesie und Grad der erforderlichen Muskelentspannung, Dauer der erforderlichen Anästhesie und körperlicher Zustand des Patienten. In allen Fällen sollte die niedrigste Konzentration und die kleinste Dosis verabreicht werden, die das gewünschte Ergebnis erzielt. Die Dosierung sollte bei Kindern, älteren und geschwächten Patienten sowie bei Patienten mit Herz- und/oder Lebererkrankungen reduziert werden.
Der Beginn der Anästhesie, die Dauer der Anästhesie und der Grad der Muskelentspannung sind proportional zum Volumen und zur Konzentration (d. h. zur Gesamtdosis) des verwendeten Lokalanästhetikums. Eine Erhöhung des Volumens und der Konzentration von Lidocainhydrochlorid-Injektion, USP, verkürzt somit den Beginn der Anästhesie, verlängert die Dauer der Anästhesie, sorgt für einen höheren Grad an Muskelentspannung und erhöht die segmentale Ausbreitung der Anästhesie. Eine Erhöhung des Volumens und der Konzentration von Lidocainhydrochlorid-Injektion, USP, kann jedoch bei der Epiduralanästhesie zu einem stärkeren Blutdruckabfall führen. Obwohl die Inzidenz von Nebenwirkungen bei Lidocain-HCl recht gering ist, ist bei der Anwendung großer Mengen und Konzentrationen Vorsicht geboten, da die Inzidenz von Nebenwirkungen direkt proportional zur Gesamtdosis des injizierten Lokalanästhetikums ist.
Für die intravenöse Regionalanästhesie sollte nur die 50-ml-Einzeldosisampulle mit Lidocain HCl 0,5% Injektion verwendet werden.
Epiduralanästhesie
Für die Epiduralanästhesie werden nur die folgenden Darreichungsformen von Lidocain HCl Injection, USP empfohlen:
| 1% ohne Epinephrin | 30mL Einzeldosis-Lösungen |
| 1% mit Epinephrin 1:200.000 | 30mL Einzeldosis-Lösungen |
| 1,5% ohne Epinephrin | 10mL Plastik-Ampulle |
| 1,5% ohne Epinephrin | 20mL Plastik-Ampulle |
| 1,5% mit Epinephrin 1:200.000 | 30mL Ampullen, 30mL Einzeldosislösungen |
| 2% ohne Epinephrin | 10mL Plastik-Ampulle |
| 2% mit Epinephrin 1:200.000 | 20-mL-Ampullen, 20-mL-Einzeldosislösungen |
Obwohl diese Lösungen speziell für die Epiduralanästhesie bestimmt sind, können sie auch für die Infiltration und die periphere Nervenblockade verwendet werden, vorausgesetzt, sie werden als Einzeldosiseinheiten eingesetzt. Diese Lösungen enthalten keine bakteriostatischen Wirkstoffe.
Bei der Epiduralanästhesie hängt die Dosierung von der Anzahl der zu betäubenden Dermatome ab (im Allgemeinen 2 bis 3 ml der angegebenen Konzentration pro Dermatom).
Kaudaler und lumbaler Epiduralblock
Als Vorsichtsmaßnahme gegen die unerwünschten Erfahrungen, die manchmal nach unbeabsichtigtem Eindringen in den Subarachnoidalraum beobachtet werden, sollte mindestens 5 Minuten vor der Injektion des Gesamtvolumens, das für eine lumbale oder kaudale Epiduralblockade erforderlich ist, eine Testdosis von z. B. 3 bis 4,5 ml 1,0 % Lidocain HCl verabreicht werden. Die Testdosis sollte wiederholt werden, wenn der Patient in einer Weise bewegt wird, die den Katheter verschoben haben könnte. Epinephrin, sofern in der Testdosis enthalten (10 bis 15 mcg wurden vorgeschlagen), kann als Warnung vor einer unbeabsichtigten intravaskulären Injektion dienen. Wenn diese Menge Epinephrin in ein Blutgefäß injiziert wird, ist es wahrscheinlich, dass sie innerhalb von 45 Sekunden eine vorübergehende "Epinephrin-Reaktion" hervorruft, die aus einem Anstieg der Herzfrequenz und des systolischen Blutdrucks, einer Blässe der Zirbeldrüse, Herzklopfen und Nervosität bei einem nicht sedierten Patienten besteht. Bei sedierten Patienten kann es sein, dass die Pulsfrequenz nur um 20 oder mehr Schläge pro Minute für 15 oder mehr Sekunden ansteigt. Patienten, die Betablocker einnehmen, zeigen möglicherweise keine Veränderungen der Herzfrequenz, aber die Blutdrucküberwachung kann einen flüchtigen Anstieg des systolischen Blutdrucks feststellen. Nach der Verabreichung jeder Testdosis sollte ausreichend Zeit für das Einsetzen der Anästhesie eingeplant werden. Die schnelle Injektion eines großen Volumens von Lidocainhydrochlorid-Injektion, USP, durch den Katheter sollte vermieden werden, und wenn möglich, sollten fraktionierte Dosen verabreicht werden.
Im Falle einer bekannten Injektion eines großen Volumens einer Lokalanästhesielösung in den Subarachnoidalraum sollte nach angemessener Reanimation und bei vorhandenem Katheter ein Versuch zur Rückgewinnung des Medikaments durch Ablassen einer moderaten Menge Liquor (z. B. 10 ml) über den Epiduralkatheter in Betracht gezogen werden.
DIE EMPFOHLENEN HÖCHSTDOSEN:
Erwachsene
Bei gesunden Erwachsenen sollte die empfohlene maximale Einzeldosis von Lidocain-HCl mit Epinephrin 7 mg/kg Körpergewicht nicht überschreiten, und im Allgemeinen wird empfohlen, dass die maximale Gesamtdosis 500 mg nicht überschreitet. Bei Anwendung ohne Epinephrin sollte die maximale Einzeldosis 4,5 mg/kg (2 mg/lb) Körpergewicht nicht überschreiten, und im Allgemeinen wird empfohlen, dass die maximale Gesamtdosis 300 mg nicht überschreitet. Bei kontinuierlicher Kaudalanästhesie sollte die empfohlene Höchstdosis nicht in Abständen von weniger als 90 Minuten verabreicht werden. Bei kontinuierlicher lumbaler oder kaudaler Epiduralanästhesie für nicht-obstruktive Eingriffe kann bei Bedarf eine höhere Dosis verabreicht werden, um eine angemessene Anästhesie zu erreichen.
Die empfohlene Höchstdosis von Lidocainhydrochlorid für die parazervikale Blockade bei geburtshilflichen und nicht geburtshilflichen Patientinnen beträgt insgesamt 200 mg pro 90 Minuten. Die Hälfte der Gesamtdosis wird in der Regel auf jeder Seite verabreicht. Die Injektion sollte langsam erfolgen, mit einem Abstand von fünf Minuten zwischen den Seiten (siehe auch die Diskussion über den parazervikalen Block in den VORSICHTSMASSNAHMEN).
Bei intravenöser Regionalanästhesie sollte die verabreichte Dosis 4 mg/kg bei Erwachsenen nicht überschreiten.
Kinder
Es ist schwierig, eine Höchstdosis für ein Medikament für Kinder zu empfehlen, da diese von Alter und Gewicht abhängt. Bei Kindern über 3 Jahren, die eine normale fettfreie Körpermasse und eine normale Körperentwicklung haben, wird die Höchstdosis durch das Alter und das Gewicht des Kindes bestimmt. Bei einem Kind von 5 Jahren und einem Gewicht von 50 Pfund sollte die Lidocain-HCl-Dosis beispielsweise 75 bis 100 mg (1,5 bis 2 mg/lb) nicht überschreiten. Für die Einleitung der intravenösen Regionalanästhesie bei Kindern wird die Verwendung noch stärker verdünnter Lösungen (d. h. 0,25 bis 0,5 %) und eine Gesamtdosis von höchstens 3 mg/kg (1,4 mg/lb) empfohlen.
Um sich vor systemischer Toxizität zu schützen, sollten stets die niedrigste wirksame Konzentration und die niedrigste wirksame Dosis verwendet werden. In einigen Fällen ist es erforderlich, die verfügbaren Konzentrationen mit 0,9%iger Natriumchlorid-Injektion zu verdünnen, um die erforderliche Endkonzentration zu erreichen.
HINWEIS: Parenterale Arzneimittel sollten vor der Verabreichung visuell auf Partikel und Verfärbungen untersucht werden, sofern die Lösung und der Behälter dies zulassen. Die Injektion darf nicht verwendet werden, wenn ihre Farbe rosa oder dunkler als leicht gelb ist oder wenn sie einen Niederschlag enthält.
Tabelle 1: Empfohlene Dosierungen für Lidocainhydrochlorid-Injektion (ohne Epinephrin)
| Infiltration | |||
| Perkutan | 0,5 oder 1 | 1 bis 60 | 5 bis 300 |
| Intravenös regional | 0.5 | 10 bis 60 | 50 bis 300 |
| Periphere Nervenblockaden, z. B, | |||
| Brachial | 1.5 | 15 bis 20 | 225 bis 300 |
| Zahnärztliche | 2 | 1 bis 5 | 20 bis 100 |
| Intercostal | 1 | 3 | 30 |
| Paravertebral | 1 | 3 bis 5 | 30 bis 50 |
| Pudendal (jede Seite) | 1 | 10 | 100 |
| Parazervikal | |||
| Analgesie bei der Geburtshilfe | |||
| (jede Seite) | 1 | 10 | 100 |
| Sympathikus-Nervenblockaden, z. B, | |||
| Zervikal (Ganglion stellatum) | 1 | 5 | 50 |
| Lendenwirbelsäule | 1 | 5 bis 10 | 50 bis 100 |
| Zentrale neuronale Blöcke | |||
| Epidural* | |||
| Thorakal | 1 | 20 bis 30 | 200 bis 300 |
| Lendenwirbelsäule | |||
| Analgesie | 1 | 25 bis 30 | 250 bis 300 |
| Anästhesie | 1.5 | 15 bis 20 | 225 bis 300 |
| 2 | 10 bis 15 | 200 bis 300 | |
| Caudal | |||
| Analgesie bei der Geburtshilfe | 1 | 20 bis 30 | 200 bis 300 |
| Chirurgische Anästhesie | 1.5 | 15 bis 20 | 225 bis 300 |
*Die Dosis richtet sich nach der Anzahl der zu betäubenden Dermatome (2-3 ml/Dermatome).
DIE OBEN VORGESCHLAGENEN KONZENTRATIONEN UND MENGEN DIENEN NUR ALS RICHTSCHNUR. ANDERE MENGEN UND KONZENTRATIONEN KÖNNEN VERWENDET WERDEN, SOFERN DIE EMPFOHLENE HÖCHSTDOSIS INSGESAMT NICHT ÜBERSCHRITTEN WIRD.
STERILISATION, LAGERUNG UND TECHNISCHE VERFAHREN:
Schwermetallhaltige Desinfektionsmittel, die entsprechende Ionen freisetzen (Quecksilber, Zink, Kupfer usw.), sollten nicht zur Haut- oder Schleimhautdesinfektion verwendet werden, da sie mit Schwellungen und Ödemen in Verbindung gebracht wurden. Wenn eine chemische Desinfektion von Mehrfachdosisfläschchen gewünscht wird, wird entweder Isopropylalkohol (91 %) oder Ethylalkohol (70 %) empfohlen. Viele im Handel erhältliche Marken von Franzbranntwein sowie Lösungen von Ethylalkohol, die nicht der USP-Qualität entsprechen, enthalten Vergällungsmittel, die für Gummi schädlich sind und daher nicht verwendet werden sollten.
WIE GELIEFERT
Lidocainhydrochlorid-Injektion, USP, wird wie folgt geliefert:
| 65282-1605-1 | Einzeldosis-Ampulle (Schachtel mit 25 Stück) | 1% (10 mg/mL) | 5 mL | 50 |
Alle Lösungen sollten bei 20° bis 25°C (68° bis 77°F) gelagert werden [siehe USP Kontrollierte Raumtemperatur].
Vor Licht schützen.
Hergestellt für:
Spectra Medical Devices, Inc.
Wilmington, MA 01887
Gebührenfrei (866) 938 - 8649
Hergestellt von:
Huons Co., Ltd,
Seoul, S. Korea
Produkt-Code: 1605-1
Überarbeitet: 03/2019
SMD-Etikett AW-0075, rev. 002
Freigegeben: 03/2019

