Informations complètes sur la prescription
Chlorhydrate de lidocaïne injectable, USSolution injectable de chlorhydrate de lidocaïne sans conservateur
Chlorhydrate de lidocaïne injectable USP, 1
Pour l'infiltration et le bloc nerveux
Rx seulement
DESCRIPTION :
Le Chlorhydrate de lidocaïne injectable, USP est une solution aqueuse stérile et apyrogène qui contient un agent anesthésique local et qui est administrée par voie parentérale par injection. Voir INDICATIONS pour les utilisations spécifiques.
La solution contient de la lidocaïne HCl, dont la dénomination chimique est acétamide, 2-(diéthylamino)-N-(2,6-diméthylphényl)-, monohydrochloride et dont le poids moléculaire est de 270,8. Le chlorhydrate de lidocaïne (C14H22N2O - HCl) a la formule structurelle suivante :
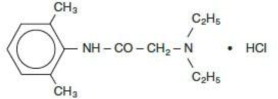
Les solutions unidoses de chlorhydrate de lidocaïne injectable, USP sont exemptes de méthylparabène.
Le chlorhydrate de lidocaïne injectable, USP est une solution isotonique stérile et apyrogène contenant du chlorure de sodium. Le pH de cette solution est ajusté à environ 6,5 (5,0 à 7,0) avec de l'hydroxyde de sodium et/ou de l'acide chlorhydrique.
LA PHARMACOLOGIE CLINIQUE :
Mécanisme d'action :
Le chlorhydrate de lidocaïne stabilise la membrane neuronale en inhibant les flux ioniques nécessaires à l'initiation et à la conduction des impulsions, ce qui entraîne une action anesthésique locale.
Hémodynamique :
Des concentrations sanguines excessives peuvent entraîner des modifications du débit cardiaque, de la résistance périphérique totale et de la pression artérielle moyenne. En cas de blocage neural central, ces modifications peuvent être attribuées au blocage des fibres autonomes, à un effet dépresseur direct de l'agent anesthésique local sur divers composants du système cardiovasculaire et/ou à l'action stimulante de l'épinéphrine sur les récepteurs bêta-adrénergiques lorsqu'elle est présente. L'effet net est normalement une hypotension modeste lorsque les doses recommandées ne sont pas dépassées.
Pharmacocinétique et métabolisme :
Les informations tirées de diverses formulations, concentrations et utilisations révèlent que le chlorhydrate de lidocaïne est complètement absorbé après administration parentérale, son taux d'absorption dépendant, par exemple, de divers facteurs tels que le site d'administration et la présence ou l'absence d'un agent vasoconstricteur. A l'exception de l'administration intravasculaire, les taux sanguins les plus élevés sont obtenus après un bloc nerveux intercostal et les plus faibles après une administration sous-cutanée.
La liaison plasmatique du chlorhydrate de lidocaïne dépend de la concentration du médicament et la fraction liée diminue avec l'augmentation de la concentration. À des concentrations de 1 à 4 mcg de base libre par mL, 60 à 80 pour cent du chlorhydrate de lidocaïne est lié aux protéines. La liaison dépend également de la concentration plasmatique de l'alpha-1-acide glycoprotéine.
Le chlorhydrate de lidocaïne traverse les barrières hémato-encéphalique et placentaire, probablement par diffusion passive.
Le chlorhydrate de lidocaïne est rapidement métabolisé par le foie, et les métabolites ainsi que le médicament inchangé sont excrétés par les reins. La biotransformation comprend la N-désalkylation oxydative, l'hydroxylation du cycle, le clivage de la liaison amide et la conjugaison. La N-désalkylation, principale voie de biotransformation, produit les métabolites monoéthylglycinexylidide et glycinexylidide. Les effets pharmacologiques/toxicologiques de ces métabolites sont similaires, mais moins puissants que ceux du chlorhydrate de lidocaïne. Environ 90 % du chlorhydrate de lidocaïne administré est excrété sous forme de divers métabolites, et moins de 10 % est excrété sous forme inchangée. Le principal métabolite dans l'urine est un conjugué de 4-hydroxy-2,6-diméthylaniline.
La demi-vie d'élimination du chlorhydrate de lidocaïne après une injection intraveineuse en bolus est généralement de 1,5 à 2 heures. En raison de la rapidité avec laquelle le chlorhydrate de lidocaïne est métabolisé, toute affection affectant la fonction hépatique peut modifier la cinétique du chlorhydrate de lidocaïne. La demi-vie peut être multipliée par deux ou plus chez les patients souffrant d'un dysfonctionnement hépatique. Le dysfonctionnement rénal n'affecte pas la cinétique du chlorhydrate de lidocaïne mais peut augmenter l'accumulation des métabolites.
Des facteurs tels que l'acidose et l'utilisation de stimulants et de dépresseurs du SNC influent sur les concentrations de chlorhydrate de lidocaïne dans le SNC nécessaires pour produire des effets systémiques manifestes. Les manifestations indésirables objectives deviennent de plus en plus apparentes lorsque les concentrations plasmatiques veineuses dépassent 6 mcg de base libre par ml. Chez le singe rhésus, il a été démontré que des concentrations sanguines artérielles de 18 à 21 mcg/mL constituaient le seuil d'activité convulsive.
INDICATIONS ET UTILISATION :
Le Chlorhydrate de lidocaïne injectable, USP est indiqué pour produire une anesthésie locale ou régionale par des techniques d'infiltration telles que l'injection percutanée et l'anesthésie régionale intraveineuse par des techniques de bloc nerveux périphérique telles que le plexus brachial et intercostal et par des techniques neurales centrales telles que les blocs épiduraux lombaires et caudaux, lorsque les procédures acceptées pour ces techniques, telles que décrites dans les manuels standard, sont respectées.
CONTRE-INDICATIONS :
Le chlorhydrate de lidocaïne est contre-indiqué chez les patients ayant des antécédents connus d'hypersensibilité aux anesthésiques locaux de type amide.
MISES EN GARDE :
LE CHLORHYDRATE DE LIDOCAÏNE INJECTABLE, USP POUR L'INFILTRATION ET LE BLOC NERVEUX NE DOIT ÊTRE UTILISÉ QUE PAR DES CLINICIENS CONNAISSANT BIEN LE DIAGNOSTIC ET LA PRISE EN CHARGE DE LA TOXICITÉ LIÉE À LA DOSE ET D'AUTRES URGENCES AIGUËS POUVANT RÉSULTER DU BLOC À UTILISER, ET SEULEMENT APRÈS S'ÊTRE ASSURÉ DE LA DISPONIBILITÉ IMMÉDIATE DE L'OXYGÈNE, D'AUTRES MÉDICAMENTS RESUSCITATIFS, DU MATÉRIEL CARDIOPULMONAIRE ET DU PERSONNEL NÉCESSAIRE POUR UNE GESTION APPROPRIÉE DES RÉACTIONS TOXIQUES ET DES URGENCES QUI EN DÉCOULENT (voir également les rubriques MISES EN GARDE ET PRÉCAUTIONS). UN RETARD DANS LA PRISE EN CHARGE DE LA TOXICITÉ LIÉE À LA DOSE, UNE SOUS-VENTILATION QUELLE QU'EN SOIT LA CAUSE ET/OU UNE ALTÉRATION DE LA SENSIBILITÉ PEUVENT CONDUIRE À L'APPARITION D'UNE ACIDOSE, D'UN ARRÊT CARDIAQUE ET, ÉVENTUELLEMENT, À LA MORT.
Méthémoglobinémie
Des cas de méthémoglobinémie ont été rapportés en association avec l'utilisation d'anesthésiques locaux. Bien que tous les patients soient exposés au risque de méthémoglobinémie, les patients présentant un déficit en glucose-6-phosphate déshydrogénase, une méthémoglobinémie congénitale ou idiopathique, une atteinte cardiaque ou pulmonaire, les nourrissons de moins de 6 mois et une exposition concomitante à des agents oxydants ou à leurs métabolites sont plus susceptibles de développer des manifestations cliniques de l'affection. Si des anesthésiques locaux doivent être utilisés chez ces patients, une surveillance étroite des symptômes et des signes de méthémoglobinémie est recommandée.
Les signes de méthémoglobinémie peuvent survenir immédiatement ou quelques heures après l'exposition et se caractérisent par une coloration cyanotique de la peau et/ou une coloration anormale du sang. Les taux de méthémoglobine peuvent continuer à augmenter ; par conséquent, un traitement immédiat est nécessaire pour éviter des effets indésirables plus graves sur le système nerveux central et le système cardiovasculaire, y compris des convulsions, le coma, des arythmies et la mort. Cesser d'administrer le chlorhydrate de lidocaïne injectable, USP et d'autres agents oxydants. Selon la gravité des signes et des symptômes, les patients peuvent répondre aux soins de soutien, c'est-à-dire à l'oxygénothérapie et à l'hydratation. Une présentation clinique plus grave peut nécessiter un traitement au bleu de méthylène, une exsanguino-transfusion ou de l'oxygène hyperbare.
Les perfusions intra-articulaires d'anesthésiques locaux à la suite d'une arthroscopie ou d'autres interventions chirurgicales ne sont pas approuvées et des cas de chondrolyse ont été signalés après la mise sur le marché chez des patients ayant reçu de telles perfusions. La majorité des cas de chondrolyse rapportés concernaient l'articulation de l'épaule ; des cas de chondrolyse gléno-humérale ont été décrits chez des patients pédiatriques et adultes après des perfusions intra-articulaires d'anesthésiques locaux avec ou sans épinéphrine pendant des périodes de 48 à 72 heures. Les informations sont insuffisantes pour déterminer si des périodes de perfusion plus courtes ne sont pas associées à ces résultats. Le moment de l'apparition des symptômes, tels que la douleur articulaire, la raideur et la perte de mouvement, peut être variable, mais peut commencer dès le deuxième mois après l'intervention chirurgicale. Actuellement, il n'existe pas de traitement efficace de la chondrolyse ; les patients qui ont souffert de chondrolyse ont dû subir des procédures diagnostiques et thérapeutiques supplémentaires et certains ont dû subir une arthroplastie ou une arthroplastie de l'épaule.
Pour éviter une injection intravasculaire, il faut procéder à une aspiration avant d'injecter la solution anesthésique locale. L'aiguille doit être repositionnée jusqu'à ce qu'aucun retour de sang ne puisse être provoqué par l'aspiration. Il convient toutefois de noter que l'absence de sang dans la seringue ne garantit pas que l'injection intravasculaire a été évitée.
Les solutions anesthésiques locales contenant des conservateurs antimicrobiens (par exemple, le méthylparabène) ne doivent pas être utilisées pour l'anesthésie péridurale ou rachidienne, car la sécurité de ces agents n'a pas été établie en ce qui concerne l'injection intrathécale, qu'elle soit intentionnelle ou accidentelle.
Les solutions de chlorhydrate de lidocaïne avec épinéphrine contiennent du métabisulfite de sodium, un sulfite qui peut provoquer des réactions de type allergique, y compris des symptômes anaphylactiques et des épisodes asthmatiques moins graves ou mettant en jeu le pronostic vital chez certaines personnes sensibles. La prévalence globale de la sensibilité aux sulfites dans la population générale est inconnue et probablement faible. La sensibilité aux sulfites est plus fréquente chez les personnes asthmatiques que chez les personnes non asthmatiques.
Des réactions anaphylactiques peuvent se produire après l'administration de chlorhydrate de lidocaïne (voir RÉACTIONS INDÉSIRABLES).
En cas de réaction grave, interrompre l'utilisation du médicament.
PRÉCAUTIONS :
Général
La sécurité et l'efficacité du chlorhydrate de lidocaïne dépendent d'un dosage approprié, d'une technique correcte, de précautions adéquates et de la préparation aux situations d'urgence. Les manuels standard doivent être consultés pour connaître les techniques et les précautions spécifiques aux différentes procédures d'anesthésie régionale.
Du matériel de réanimation, de l'oxygène et d'autres médicaments de réanimation doivent être disponibles pour une utilisation immédiate. (Voir MISES EN GARDE et EFFETS INDÉSIRABLES). La dose la plus faible permettant d'obtenir une anesthésie efficace doit être utilisée afin d'éviter des taux plasmatiques élevés et des effets indésirables graves. Des aspirations de seringue doivent également être effectuées avant et pendant chaque injection supplémentaire lors de l'utilisation de techniques de cathéters à demeure. Lors de l'administration d'une anesthésie péridurale, il est recommandé d'administrer initialement une dose test et de surveiller le patient pour déceler toute toxicité sur le système nerveux central et sur le système cardiovasculaire, ainsi que tout signe d'administration intrathécale involontaire, avant de poursuivre. Lorsque les conditions cliniques le permettent, il faut envisager d'utiliser des solutions d'anesthésiques locaux contenant de l'épinéphrine pour la dose test, car les modifications circulatoires compatibles avec l'épinéphrine peuvent également servir de signe d'alerte d'une injection intravasculaire involontaire. Une injection intravasculaire est toujours possible même si les aspirations sanguines sont négatives. Des doses répétées de chlorhydrate de lidocaïne peuvent entraîner des augmentations significatives des taux sanguins à chaque dose répétée en raison de l'accumulation lente du médicament ou de ses métabolites. La tolérance à des taux sanguins élevés varie en fonction de l'état du patient. Les patients affaiblis, les personnes âgées, les patients souffrant d'une maladie aiguë et les enfants doivent recevoir des doses réduites en fonction de leur âge et de leur condition physique. Le chlorhydrate de lidocaïne doit également être utilisé avec prudence chez les patients en état de choc grave ou présentant un bloc cardiaque.
L'anesthésie épidurale lombaire et caudale doit être utilisée avec une extrême prudence chez les personnes présentant les conditions suivantes : maladie neurologique existante, déformations de la colonne vertébrale, septicémie et hypertension sévère.
Les solutions anesthésiques locales contenant un vasoconstricteur doivent être utilisées avec prudence et en quantités soigneusement circonscrites dans les zones du corps irriguées par des artères terminales ou dont l'irrigation sanguine est autrement compromise. Les patients souffrant d'une maladie vasculaire périphérique ou d'une maladie vasculaire hypertensive peuvent présenter une réponse vasoconstrictrice exagérée. Des lésions ischémiques ou une nécrose peuvent en résulter. Les préparations contenant un vasoconstricteur doivent être utilisées avec prudence chez les patients pendant ou après l'administration d'agents anesthésiques généraux puissants, car des arythmies cardiaques peuvent survenir dans ces conditions.
Une surveillance attentive et constante des signes vitaux cardiovasculaires et respiratoires (adéquation de la ventilation) et de l'état de conscience du patient doit être effectuée après chaque injection d'anesthésique local. Il faut alors garder à l'esprit que l'agitation, l'anxiété, les acouphènes, les vertiges, la vision trouble, les tremblements, la dépression ou la somnolence peuvent être des signes précurseurs d'une toxicité pour le système nerveux central.
Comme les anesthésiques locaux de type amide sont métabolisés par le foie, le Chlorhydrate de lidocaïne injectable, USP doit être utilisé avec prudence chez les patients atteints d'une maladie hépatique. Les patients atteints d'une maladie hépatique grave, en raison de leur incapacité à métaboliser normalement les anesthésiques locaux, risquent davantage de présenter des concentrations plasmatiques toxiques. Le Chlorhydrate de lidocaïne injectable, USP doit également être utilisé avec prudence chez les patients dont la fonction cardiovasculaire est altérée, car ils peuvent être moins en mesure de compenser les changements fonctionnels associés à l'allongement de la conduction auriculo-ventriculaire produit par ces médicaments.
De nombreux médicaments utilisés pendant l'anesthésie sont considérés comme des agents déclencheurs potentiels de l'hyperthermie maligne familiale. Comme on ne sait pas si les anesthésiques locaux de type amide peuvent déclencher cette réaction et que la nécessité d'une anesthésie générale supplémentaire ne peut être prévue à l'avance, il est suggéré de disposer d'un protocole standard pour la prise en charge de l'hyperthermie maligne. Des signes précoces et inexpliqués de tachycardie, de tachypnée, de tension artérielle instable et d'acidose métabolique peuvent précéder l'élévation de la température. L'issue positive dépend d'un diagnostic précoce, de l'arrêt rapide du ou des agents déclencheurs suspects et de l'instauration d'un traitement, y compris l'oxygénothérapie, les mesures de soutien indiquées et le dantrolène (consulter la notice du dantrolène sodique intraveineux avant de l'utiliser).
Une bonne technique de garrot, telle que décrite dans les publications et les manuels standard, est essentielle pour la réalisation d'une anesthésie régionale par voie intraveineuse. Les solutions contenant de l'épinéphrine ou d'autres vasoconstricteurs ne doivent pas être utilisées pour cette technique.
Le chlorhydrate de lidocaïne doit être utilisé avec prudence chez les personnes présentant des sensibilités médicamenteuses connues. Les patients allergiques aux dérivés de l'acide para-aminobenzoïque (procaïne, tétracaïne, benzocaïne, etc.) n'ont pas montré de sensibilité croisée au chlorhydrate de lidocaïne.
Utilisation dans la région de la tête et du cou
L'injection de petites doses d'anesthésiques locaux dans la région de la tête et du cou, y compris les blocs rétrobulbaires, dentaires et du ganglion stellaire, peut produire des effets indésirables similaires à la toxicité systémique observée lors d'injections intravasculaires involontaires de doses plus importantes. Des cas de confusion, de convulsions, de dépression respiratoire et/ou d'arrêt respiratoire, ainsi que de stimulation ou de dépression cardiovasculaire ont été rapportés. Ces réactions peuvent être dues à l'injection intra-artérielle de l'anesthésique local avec un flux rétrograde vers la circulation cérébrale. La circulation et la respiration des patients recevant ces blocs doivent être surveillées et faire l'objet d'une observation constante. Le matériel de réanimation et le personnel chargé de traiter les effets indésirables doivent être immédiatement disponibles. La posologie recommandée ne doit pas être dépassée (voir POSOLOGIE ET ADMINISTRATION).
Informations pour les patients
Le cas échéant, les patients doivent être informés à l'avance qu'ils peuvent ressentir une perte temporaire de sensation et d'activité motrice, généralement dans la moitié inférieure du corps, après l'administration correcte de l'anesthésie péridurale.
Interactions médicamenteuses cliniquement significatives
L'administration de solutions anesthésiques locales contenant de l'épinéphrine ou de la norépinéphrine à des patients recevant des inhibiteurs de la monoamine oxydase ou des antidépresseurs tricycliques peut provoquer une hypertension sévère et prolongée.
Les phénothiazines et les butyrophénones peuvent réduire ou inverser l'effet pressant de l'épinéphrine.
L'utilisation simultanée de ces agents doit généralement être évitée. Dans les cas où un traitement concomitant est nécessaire, il est essentiel de surveiller attentivement le patient.
L'administration simultanée de médicaments vasopresseurs (pour le traitement de l'hypotension liée aux blocs obstétricaux) et de médicaments ocytociques de type ergot peut provoquer une hypertension sévère et persistante ou des accidents vasculaires cérébraux.
Interactions entre les médicaments et les tests de laboratoire
L'injection intramusculaire de lidocaïne HCl peut entraîner une augmentation des taux de créatine phosphokinase. Ainsi, l'injection intramusculaire de lidocaïne HCl peut compromettre l'utilisation de ce dosage enzymatique, sans séparation des isoenzymes, comme test diagnostique de la présence d'un infarctus aigu du myocarde.
Les patients auxquels on administre des anesthésiques locaux courent un risque accru de développer une méthémoglobinémie en cas d'exposition simultanée aux médicaments suivants, qui peuvent inclure d'autres anesthésiques locaux :
Exemples de médicaments associés à la méthémoglobinémie :
| Nitrates/Nitrites | Oxyde nitrique, nitroglycérine, nitroprussiate, oxyde nitreux |
| Anesthésiques locaux | Articane, benzocaïne, bupivacaïne, lidocaïne, mépivacaïne, prilocaïne, procaïne, ropivacaïne, tétracaïne |
| Agents antinéoplasiques | Cyclophosphamide, flutamide, hydroxyurée, ifosfamide, rasburicase |
| Antibiotiques | Dapsone, nitrofurantoïne, acide para-aminosalicylique, sulfamides |
| Antimalariques | Choloroquine, primaquine |
| Anticonvulsivants | Phénobarbital, phénytoïne, valproate de sodium |
| Autres médicaments | Acétaminophène, métoclopramide, quinine, sulfasalazine |
Carcinogenèse, mutagenèse, altération de la fertilité
Le chlorhydrate de lidocaïne n'a pas fait l'objet d'études chez l'animal pour évaluer son potentiel cancérigène et mutagène ou son effet sur la fertilité.
Grossesse
Effets tératogènes : Catégorie de grossesse B.
Des études de reproduction ont été réalisées chez le rat à des doses allant jusqu'à 6,6 fois la dose humaine et n'ont révélé aucun signe d'effets nocifs pour le fœtus causés par le chlorhydrate de lidocaïne. Il n'existe cependant pas d'études adéquates et bien contrôlées chez la femme enceinte. Les études sur la reproduction animale ne permettent pas toujours de prédire la réaction humaine. Il convient d'en tenir compte avant d'administrer le chlorhydrate de lidocaïne à des femmes en âge de procréer, en particulier au début de la grossesse, lorsque l'organogenèse est à son maximum.
Travail et accouchement
Les anesthésiques locaux traversent rapidement le placenta et, lorsqu'ils sont utilisés pour l'anesthésie péridurale, paracervicale, pudendale ou caudale, ils peuvent entraîner divers degrés de toxicité maternelle, fœtale et néonatale (voir PHARMACOLOGIE CLINIQUE, Pharmacocinétique et métabolisme). (voir PHARMACOLOGIE CLINIQUE, Pharmacocinétique et métabolisme). Le risque de toxicité dépend de l'intervention pratiquée, du type et de la quantité de médicament utilisé et de la technique d'administration. Les effets indésirables chez la parturiente, le fœtus et le nouveau-né impliquent des altérations du système nerveux central, du tonus vasculaire périphérique et de la fonction cardiaque.
L'anesthésie régionale a entraîné une hypotension maternelle. Les anesthésiques locaux produisent une vasodilatation en bloquant les nerfs sympathiques. Le fait de surélever les jambes de la patiente et de la positionner sur le côté gauche permet d'éviter une baisse de la tension artérielle.
Le rythme cardiaque du fœtus doit également être surveillé en permanence, et la surveillance électronique du fœtus est fortement conseillée.
L'anesthésie péridurale, rachidienne, paracervicale ou pudendale peut modifier les forces de la parturition par des changements dans la contractilité utérine ou les efforts d'expulsion de la mère. Dans une étude, l'anesthésie par bloc paracervical a été associée à une diminution de la durée moyenne du premier stade du travail et à une facilitation de la dilatation cervicale. Cependant, il a également été rapporté que l'anesthésie rachidienne et péridurale prolongeait la deuxième phase du travail en supprimant le besoin réflexe de la parturiente de se baisser ou en interférant avec la fonction motrice. Le recours à l'anesthésie obstétricale peut augmenter la nécessité d'une assistance par forceps.
L'utilisation de certains anesthésiques locaux pendant le travail et l'accouchement peut être suivie d'une diminution de la force et du tonus musculaire pendant le premier ou les deux premiers jours de la vie. La signification à long terme de ces observations est inconnue. Une bradycardie fœtale peut survenir chez 20 à 30 % des patientes recevant une anesthésie par bloc nerveux paracervical avec des anesthésiques locaux de type amide et peut être associée à une acidose fœtale. Le rythme cardiaque fœtal doit toujours être surveillé pendant l'anesthésie paracervicale. Le médecin doit évaluer les avantages possibles par rapport aux risques lorsqu'il envisage un bloc paracervical en cas de prématurité, de toxémie gravidique et de détresse fœtale. Le respect scrupuleux de la posologie recommandée est de la plus haute importance pour le bloc paracervical obstétrical. L'impossibilité d'obtenir une analgésie adéquate avec les doses recommandées doit faire suspecter une injection intravasculaire ou intracrânienne fœtale. Des cas compatibles avec une injection intracrânienne fœtale involontaire d'une solution anesthésique locale ont été rapportés après un bloc paracervical ou pudendal intentionnel ou les deux. Les bébés ainsi affectés présentent une dépression néonatale inexpliquée à la naissance, qui est en corrélation avec des taux sériques élevés d'anesthésique local, et manifestent souvent des convulsions dans les six heures qui suivent. L'application rapide de mesures de soutien combinée à l'excrétion urinaire forcée de l'anesthésique local a été utilisée avec succès pour gérer cette complication.
Des rapports de cas de convulsions maternelles et de collapsus cardiovasculaire suite à l'utilisation de certains anesthésiques locaux pour le bloc paracervical en début de grossesse (comme anesthésie pour un avortement électif) suggèrent que l'absorption systémique dans ces circonstances peut être rapide. La dose maximale recommandée pour chaque médicament ne doit pas être dépassée. L'injection doit être faite lentement et avec une aspiration fréquente. Respecter un intervalle de 5 minutes entre chaque côté.
Allaitement
On ne sait pas si ce médicament est excrété dans le lait maternel. Étant donné que de nombreux médicaments sont excrétés dans le lait maternel, il convient d'être prudent lorsque le chlorhydrate de lidocaïne est administré à une femme qui allaite.
Utilisation en pédiatrie
Chez les enfants, les doses doivent être réduites en fonction de l'âge, du poids corporel et de la condition physique (voir POSOLOGIE ET ADMINISTRATION).
LES EFFETS INDÉSIRABLES
Systémique
Les effets indésirables consécutifs à l'administration de chlorhydrate de lidocaïne sont de nature similaire à ceux observés avec d'autres anesthésiques locaux de type amide. Ces effets indésirables sont généralement liés à la dose et peuvent résulter de taux plasmatiques élevés dus à un dosage excessif, à une absorption rapide ou à une injection intravasculaire accidentelle, ou peuvent résulter d'une hypersensibilité, d'une idiosyncrasie ou d'une tolérance diminuée de la part du patient. Les effets indésirables graves sont généralement de nature systémique. Les types suivants sont les plus fréquemment rapportés :
Système nerveux central
Les manifestations du SNC sont excitatrices et/ou dépressives et peuvent être caractérisées par des vertiges, de la nervosité, de l'appréhension, de l'euphorie, de la confusion, des étourdissements, de la somnolence, des acouphènes, une vision floue ou double, des vomissements, des sensations de chaleur, de froid ou d'engourdissement, des contractions, des tremblements, des convulsions, une perte de conscience, une dépression respiratoire et un arrêt respiratoire. Les manifestations excitatrices peuvent être très brèves ou ne pas se produire du tout, auquel cas la première manifestation de toxicité peut être une somnolence se transformant en perte de conscience et en arrêt respiratoire.
La somnolence consécutive à l'administration de chlorhydrate de lidocaïne est généralement un signe précoce d'une concentration sanguine élevée du médicament et peut être la conséquence d'une absorption rapide.
Système cardiovasculaire
Les manifestations cardiovasculaires sont généralement dépressives et se caractérisent par une bradycardie, une hypotension et un collapsus cardiovasculaire pouvant conduire à un arrêt cardiaque.
Allergique
Les réactions allergiques se caractérisent par des lésions cutanées, de l'urticaire, un œdème ou des réactions anaphylactoïdes. Les réactions allergiques peuvent résulter d'une sensibilité soit aux agents anesthésiques locaux, soit au méthylparabène utilisé comme conservateur dans les flacons multidoses. Des réactions allergiques, y compris des réactions anaphylactiques, peuvent survenir à la suite d'une sensibilité à la lidocaïne, mais elles sont peu fréquentes. Si des réactions allergiques se produisent, elles doivent être traitées par des moyens conventionnels. La détection de la sensibilité par des tests cutanés est d'une valeur douteuse.
Aucun cas de sensibilité croisée entre le chlorhydrate de lidocaïne et le procaïnamide ou entre le chlorhydrate de lidocaïne et la quinidine n'a été signalé.
Neurologique
L'incidence des effets indésirables associés à l'utilisation d'anesthésiques locaux peut être liée à la dose totale d'anesthésique local administrée et dépend également du médicament utilisé, de la voie d'administration et de l'état physique du patient. Dans une étude prospective portant sur 10 440 patients ayant reçu du chlorhydrate de lidocaïne pour une anesthésie rachidienne, l'incidence des effets indésirables a été rapportée à environ 3 % pour les céphalées de position, l'hypotension et les maux de dos, à 2 % pour les frissons et à moins de 1 % pour les symptômes des nerfs périphériques, les nausées, l'insuffisance respiratoire et la vision double. Nombre de ces observations peuvent être liées aux techniques d'anesthésie locale, avec ou sans contribution de l'anesthésique local.
Dans la pratique du bloc péridural caudal ou lombaire, une pénétration accidentelle occasionnelle de l'espace sous-arachnoïdien par le cathéter peut se produire. Les effets indésirables ultérieurs peuvent dépendre en partie de la quantité de médicament administrée par voie sous-durale. Il peut s'agir d'un bloc spinal de magnitude variable (y compris un bloc spinal total), d'une hypotension secondaire au bloc spinal, d'une perte de contrôle de la vessie et des intestins, et d'une perte de la sensibilité périnéale et de la fonction sexuelle. Un déficit moteur, sensoriel et/ou autonome (contrôle du sphincter) persistant de certains segments spinaux inférieurs avec une récupération lente (plusieurs mois) ou incomplète a été rapporté dans de rares cas lorsque le bloc épidural caudal ou lombaire a été tenté. Des maux de dos et des céphalées ont également été observés après l'utilisation de ces procédures anesthésiques.
Des cas de lésions permanentes des muscles extraoculaires nécessitant une réparation chirurgicale après administration rétrobulbaire ont été rapportés.
Hématologie
Méthémoglobinémie.
SURDOSAGE
Les urgences aiguës provoquées par les anesthésiques locaux sont généralement liées à des concentrations plasmatiques élevées observées lors de l'utilisation thérapeutique des anesthésiques locaux ou à l'injection sous-arachnoïdienne involontaire d'une solution d'anesthésique local (voir EFFETS INDÉSIRABLES, MISES EN GARDE et PRÉCAUTIONS).
Prise en charge des urgences anesthésiques locales
La première considération est la prévention, qui est le mieux réalisée par une surveillance attentive et constante des signes vitaux cardiovasculaires et respiratoires et de l'état de conscience du patient après chaque injection d'anesthésique local. Au premier signe de changement, de l'oxygène doit être administré.
La première étape de la prise en charge des convulsions, ainsi que de la sous-ventilation ou de l'apnée due à l'injection sous-arachnoïdienne involontaire d'une solution médicamenteuse, consiste à veiller immédiatement au maintien de la perméabilité des voies aériennes et à la ventilation assistée ou contrôlée avec de l'oxygène et un système d'administration capable de permettre une pression positive immédiate des voies aériennes au moyen d'un masque. Immédiatement après la mise en place de ces mesures ventilatoires, il convient d'évaluer l'adéquation de la circulation, en gardant à l'esprit que les médicaments utilisés pour traiter les convulsions dépriment parfois la circulation lorsqu'ils sont administrés par voie intraveineuse. Si les convulsions persistent malgré une assistance respiratoire adéquate, et si l'état de la circulation le permet, de petites doses d'un barbiturique à action ultra-courte (comme le thiopental ou le thiamylal) ou d'une benzodiazépine (comme le diazépam) peuvent être administrées par voie intraveineuse. Avant d'utiliser des anesthésiques locaux, le clinicien doit être familiarisé avec ces médicaments anticonvulsivants. Le traitement de soutien de la dépression circulatoire peut nécessiter l'administration de fluides intraveineux et, le cas échéant, d'un vasopresseur en fonction de la situation clinique (par exemple, éphédrine).
Si elles ne sont pas traitées immédiatement, les convulsions et la dépression cardiovasculaire peuvent entraîner une hypoxie, une acidose, une bradycardie, des arythmies et un arrêt cardiaque. Une sous-ventilation ou une apnée due à une injection sous-arachnoïdienne involontaire de solution anesthésique locale peut produire ces mêmes signes et entraîner un arrêt cardiaque si une assistance respiratoire n'est pas mise en place. En cas d'arrêt cardiaque, les mesures de réanimation cardio-pulmonaire standard doivent être mises en œuvre.
L'intubation endotrachéale, utilisant des médicaments et des techniques familières au clinicien, peut être indiquée, après l'administration initiale d'oxygène au masque, en cas de difficulté à maintenir la perméabilité des voies aériennes ou si une assistance respiratoire prolongée (assistée ou contrôlée) est indiquée.
La dialyse est d'une valeur négligeable dans le traitement d'un surdosage aigu en chlorhydrate de lidocaïne. La DL50 orale du chlorhydrate de lidocaïne chez les rats femelles non à jeun est de 459 (346 à 773) mg/kg (sous forme de sel) et de 214 (159 à 324) mg/kg (sous forme de sel) chez les rats femelles à jeun.
DOSAGE ET ADMINISTRATION
Le tableau 1 (Posologies recommandées) résume les volumes et les concentrations de Chlorhydrate de lidocaïne injectable, USP recommandés pour divers types d'anesthésies. Les doses suggérées dans ce tableau s'appliquent à des adultes en bonne santé et se rapportent à l'utilisation de solutions contenant de l'épinéphrine. Lorsque des volumes plus importants sont nécessaires, seules les solutions contenant de l'épinéphrine doivent être utilisées, sauf dans les cas où les médicaments vasopresseurs peuvent être contre-indiqués.
On a signalé des cas de chondrolyse chez des patients recevant des perfusions intra-articulaires d'anesthésiques locaux à la suite d'une arthroscopie ou d'autres interventions chirurgicales. Le Chlorhydrate de lidocaïne injectable, USP n'est pas approuvé pour cet usage (voir MISES EN GARDE et POSOLOGIE ET ADMINISTRATION).
Ces doses recommandées ne servent que de guide pour la quantité d'anesthésique nécessaire pour la plupart des interventions de routine. Les volumes et concentrations réels à utiliser dépendent d'un certain nombre de facteurs tels que le type et l'étendue de l'intervention chirurgicale, la profondeur de l'anesthésie et le degré de relaxation musculaire requis, la durée de l'anesthésie requise et l'état physique du patient. Dans tous les cas, il convient d'administrer la plus faible concentration et la plus petite dose permettant d'obtenir le résultat souhaité. Les doses doivent être réduites pour les enfants, les personnes âgées, les patients affaiblis et les patients souffrant de maladies cardiaques et/ou hépatiques.
Le début de l'anesthésie, la durée de l'anesthésie et le degré de relaxation musculaire sont proportionnels au volume et à la concentration (c.-à-d. la dose totale) de l'anesthésique local utilisé. Ainsi, une augmentation du volume et de la concentration de Chlorhydrate de lidocaïne injectable, USP réduira l'apparition de l'anesthésie, prolongera la durée de l'anesthésie, procurera un plus grand degré de relaxation musculaire et augmentera l'étendue segmentaire de l'anesthésie. Toutefois, l'augmentation du volume et de la concentration du Chlorhydrate de lidocaïne injectable, USP peut entraîner une chute plus importante de la tension artérielle lors de l'anesthésie péridurale. Bien que l'incidence des effets secondaires du chlorhydrate de lidocaïne soit assez faible, il faut faire preuve de prudence lorsqu'on utilise de grands volumes et de grandes concentrations, car l'incidence des effets secondaires est directement proportionnelle à la dose totale d'agent anesthésique local injectée.
Pour l'anesthésie régionale intraveineuse, seul le flacon unidose de 50 ml contenant du chlorhydrate de lidocaïne 0,5 % injectable doit être utilisé.
Anesthésie péridurale
Pour l'anesthésie épidurale, seules les formes posologiques suivantes de chlorhydrate de lidocaïne injectable, USP sont recommandées :
| 1% sans épinéphrine | Solutions à dose unique de 30 ml |
| 1% avec épinéphrine 1:200 000 | Solutions à dose unique de 30 ml |
| 1,5 % sans épinéphrine | Ampoule en plastique de 10 ml |
| 1,5 % sans épinéphrine | Ampoule en plastique de 20 ml |
| 1,5 % avec épinéphrine 1:200 000 | Ampoules de 30 ml, solutions à dose unique de 30 ml |
| 2% sans épinéphrine | Ampoule en plastique de 10 ml |
| 2 % avec épinéphrine 1:200 000 | Ampoules de 20 ml, solutions à dose unique de 20 ml |
Bien que ces solutions soient destinées spécifiquement à l'anesthésie péridurale, elles peuvent également être utilisées pour l'infiltration et le bloc nerveux périphérique, à condition d'être employées en doses uniques. Ces solutions ne contiennent pas d'agent bactériostatique.
En anesthésie péridurale, la posologie varie en fonction du nombre de dermatomes à anesthésier (généralement 2 à 3 ml de la concentration indiquée par dermatome).
Bloc péridural caudal et lombaire
En guise de précaution contre les effets indésirables parfois observés à la suite d'une pénétration involontaire dans l'espace sous-arachnoïdien, une dose test telle que 3 à 4,5 ml de chlorhydrate de lidocaïne à 1,0 % doit être administrée au moins 5 minutes avant l'injection du volume total requis pour un bloc péridural lombaire ou caudal. La dose test doit être répétée si le patient est déplacé d'une manière susceptible d'avoir déplacé le cathéter. L'épinéphrine, si elle est contenue dans la dose test (10 à 15 mcg ont été suggérés), peut servir d'avertissement en cas d'injection intravasculaire involontaire. Si elle est injectée dans un vaisseau sanguin, cette quantité d'épinéphrine est susceptible de produire une "réponse épinéphrine" transitoire en 45 secondes, consistant en une augmentation de la fréquence cardiaque et de la pression artérielle systolique, une pâleur circulatoire, des palpitations et de la nervosité chez le patient non sédaté. Le patient sous sédatifs peut ne présenter qu'une augmentation du pouls de 20 battements par minute ou plus pendant 15 secondes ou plus. Les patients sous bêta-bloquants peuvent ne pas manifester de changements dans leur fréquence cardiaque, mais la surveillance de la pression artérielle peut détecter une augmentation évanescente de la pression artérielle systolique. Il convient de prévoir un délai suffisant pour l'apparition de l'anesthésie après l'administration de chaque dose test. Il faut éviter d'injecter rapidement un grand volume de Chlorhydrate de lidocaïne injectable, USP dans le cathéter et, dans la mesure du possible, administrer des doses fractionnées.
En cas d'injection connue d'un grand volume de solution anesthésique locale dans l'espace sous-arachnoïdien, après une réanimation appropriée et si le cathéter est en place, envisagez de tenter de récupérer le médicament en drainant une quantité modérée de liquide céphalorachidien (par exemple 10 ml) par le cathéter péridural.
LES DOSES MAXIMALES RECOMMANDÉES :
Adultes
Pour les adultes en bonne santé, la dose individuelle maximale recommandée de chlorhydrate de lidocaïne avec épinéphrine ne doit pas dépasser 7 mg/kg (3,5 mg/lb) de poids corporel et, en général, il est recommandé que la dose totale maximale ne dépasse pas 500 mg. Lorsqu'il est utilisé sans épinéphrine, la dose individuelle maximale ne doit pas dépasser 4,5 mg/kg (2 mg/lb) de poids corporel et, en général, il est recommandé que la dose totale maximale ne dépasse pas 300 mg. Pour l'anesthésie caudale continue, la dose maximale recommandée ne doit pas être administrée à des intervalles inférieurs à 90 minutes. Lorsque l'anesthésie péridurale lombaire ou caudale continue est utilisée pour des interventions non obstétricales, une plus grande quantité de médicament peut être administrée si nécessaire pour produire une anesthésie adéquate.
La dose maximale recommandée par période de 90 minutes de chlorhydrate de lidocaïne pour le bloc paracervical chez les patientes obstétricales et non obstétricales est de 200 mg au total. La moitié de la dose totale est généralement administrée de chaque côté. Injecter lentement, en respectant un intervalle de cinq minutes entre les côtés (voir également la discussion sur le bloc paracervical dans les PRÉCAUTIONS).
Pour l'anesthésie régionale par voie intraveineuse, la dose administrée ne doit pas dépasser 4 mg/kg chez l'adulte.
Les enfants
Il est difficile de recommander une dose maximale de médicament pour les enfants, car celle-ci varie en fonction de l'âge et du poids. Pour les enfants de plus de 3 ans qui ont une masse corporelle maigre normale et un développement corporel normal, la dose maximale est déterminée par l'âge et le poids de l'enfant. Par exemple, chez un enfant de 5 ans pesant 50 livres, la dose de chlorhydrate de lidocaïne ne doit pas dépasser 75 à 100 mg (1,5 à 2 mg/lb). L'utilisation de solutions encore plus diluées (c'est-à-dire de 0,25 à 0,5 %) et des doses totales ne dépassant pas 3 mg/kg (1,4 mg/lb) sont recommandées pour l'induction de l'anesthésie régionale intraveineuse chez les enfants.
Afin de se prémunir contre la toxicité systémique, la concentration efficace la plus faible et la dose efficace la plus faible doivent être utilisées à tout moment. Dans certains cas, il sera nécessaire de diluer les concentrations disponibles dans une solution injectable de chlorure de sodium à 0,9 % afin d'obtenir la concentration finale requise.
REMARQUE : Les médicaments pour usage parentéral doivent être inspectés visuellement avant l'administration pour vérifier qu'ils ne contiennent pas de particules et qu'ils ne sont pas décolorés, lorsque la solution et le récipient le permettent. La solution injectable ne doit pas être utilisée si sa couleur est rosâtre ou plus foncée que légèrement jaune ou si elle contient un précipité.
Tableau 1 : Doses recommandées pour le chlorhydrate de lidocaïne injectable (sans épinéphrine)
| Infiltration | |||
| Par voie percutanée | 0,5 ou 1 | 1 à 60 | 5 à 300 |
| Régionale intraveineuse | 0.5 | 10 à 60 | 50 à 300 |
| Blocs nerveux périphériques, par exemple, | |||
| Brachial | 1.5 | 15 à 20 | 225 à 300 |
| Soins dentaires | 2 | 1 à 5 | 20 à 100 |
| Intercostal | 1 | 3 | 30 |
| Paravertébrale | 1 | 3 à 5 | 30 à 50 |
| Pudendal (chaque côté) | 1 | 10 | 100 |
| Paracervical | |||
| Analgésie obstétricale | |||
| (de chaque côté) | 1 | 10 | 100 |
| Blocs des nerfs sympathiques, par exemple, | |||
| Cervical (ganglion stellaire) | 1 | 5 | 50 |
| Lombaire | 1 | 5 à 10 | 50 à 100 |
| Blocs neuronaux centraux | |||
| La péridurale* | |||
| Thoracique | 1 | 20 à 30 | 200 à 300 |
| Lombaire | |||
| Analgésie | 1 | 25 à 30 | 250 à 300 |
| Anesthésie | 1.5 | 15 à 20 | 225 à 300 |
| 2 | 10 à 15 ans | 200 à 300 | |
| Caudale | |||
| Analgésie obstétricale | 1 | 20 à 30 | 200 à 300 |
| Anesthésie chirurgicale | 1.5 | 15 à 20 | 225 à 300 |
*La dose est déterminée par le nombre de dermatomes à anesthésier (2-3 ml/dermatome).
LES CONCENTRATIONS ET VOLUMES SUGGÉRÉS CI-DESSUS NE SONT DONNÉS QU'À TITRE INDICATIF. D'AUTRES VOLUMES ET CONCENTRATIONS PEUVENT ÊTRE UTILISÉS À CONDITION QUE LA DOSE TOTALE MAXIMALE RECOMMANDÉE NE SOIT PAS DÉPASSÉE.
LA STÉRILISATION, LE STOCKAGE ET LES PROCÉDURES TECHNIQUES :
Les agents désinfectants contenant des métaux lourds, qui provoquent la libération d'ions respectifs (mercure, zinc, cuivre, etc.), ne doivent pas être utilisés pour la désinfection de la peau ou des muqueuses, car ils ont été associés à des incidents de gonflement et d'œdème. Lorsqu'une désinfection chimique des flacons multidoses est souhaitée, il est recommandé d'utiliser de l'alcool isopropylique (91 %) ou de l'alcool éthylique (70 %). De nombreuses marques d'alcool à friction disponibles dans le commerce, ainsi que des solutions d'alcool éthylique qui ne sont pas de qualité USP, contiennent des dénaturants qui sont nocifs pour le caoutchouc et ne doivent donc pas être utilisés.
MODE D'APPROVISIONNEMENT
Le Chlorhydrate de lidocaïne injectable, USP est présenté comme suit :
| 65282-1605-1 | Ampoule à dose unique (boîte de 25) | 1 % (10 mg/mL) | 5 ml | 50 |
Toutes les solutions doivent être conservées à une température comprise entre 20 et 25 °C (68 et 77 °F) [voir USP Controlled Room Temperature].
Protéger de la lumière.
Fabriqué pour :
Spectra Medical Devices, Inc.
Wilmington, MA 01887
Numéro gratuit (866) 938 - 8649
Fabriqué par :
Huons Co,
Séoul, Corée du Sud
Code produit : 1605-1
Révisé : 03/2019
Étiquette SMD AW-0075, rév. 002
Diffusé : 03/2019

